由于新病例的迅速增加,2019年冠状病毒病(COVID-19)很快引起了全球关注,病原体被鉴定为SARS-CoV-2。截至目前(5月17日),据约翰·霍普金斯大学发布的实时统计数据,全球累计新冠肺炎确诊病例超过470万例,死亡人数达31万。这些数字每天都会更新,而且预计还会进一步增加。但是,现在一直缺乏动物模型,这严重阻碍了药物及疫苗的研发。
2020年5月21日,中科院武汉病毒所石正丽及杨兴娄共同通讯在Cell在线发表题为“Pathogenesis of SARS-CoV-2 in transgenic mice expressing human angiotensin-converting enzyme 2”的研究论文,该研究成功开发了SARS-CoV-2 hACE2转基因小鼠(在C3B6小鼠中为HFH4-hACE2)感染模型。感染的小鼠产生典型的间质性肺炎和病理,与COVID-19患者相似。病毒定量显示肺是感染的主要部位,尽管在某些小鼠的眼睛,心脏和大脑中也可以发现病毒RNA。从感染的肺和脑组织中分离出全基因组序列中与SARS-CoV-2相同的病毒。最后,该研究表明预先暴露于SARS-CoV-2可以保护小鼠免受严重的肺炎的侵害。总而言之,该结果表明,hACE2小鼠将成为测试潜在疫苗和治疗剂的有价值的工具。
另外,2020年5月7日,北京协和医学院秦川及中国疾病预防控制中心病毒病预防控制所武桂珍共同通讯在Nature在线发表题为“The pathogenicity of SARS-CoV-2 in hACE2 transgenic mice”的研究论文,该研究使用感染SARS-CoV-2的hACE2转基因小鼠研究病毒的致病性。在感染SARS-CoV-2的hACE2小鼠中观察到了体重减轻和病毒在肺中复制。典型的组织病理学是间质性肺炎,肺泡间质中大量淋巴细胞和单核细胞浸润,肺泡腔内巨噬细胞聚集。在支气管上皮细胞,肺泡巨噬细胞和肺泡上皮细胞中观察到病毒抗原。在具有SARS-CoV-2感染的野生型小鼠(没有转hACE2的小鼠)中未发现该现象。该研究阐明了hACE2小鼠中SARS-CoV-2的致病性,并满足了Koch的假设,该小鼠模型可促进针对SARS-CoV-2的疗法和疫苗的开发(点击阅读)。

由于新病例的迅速增加,2019年冠状病毒病(COVID-19)很快引起了全球关注。新型冠状病毒感染被认为是从动物传播的,病原体被鉴定为SARS-CoV-2。到2020年1月,怀疑最初受感染的患者是通过人与人之间的传播感染了该病毒。自2020年1月以来,该病毒已迅速传播到中国大部分地区和其他国家。
由于新病例的迅速增加,2019年冠状病毒病(COVID-19)很快引起了全球关注,病原体被鉴定为SARS-CoV-2。截至目前(5月17日),据约翰·霍普金斯大学发布的实时统计数据,全球累计新冠肺炎确诊病例超过470万例,死亡人数达31万。这些数字每天都会更新,而且预计还会进一步增加。
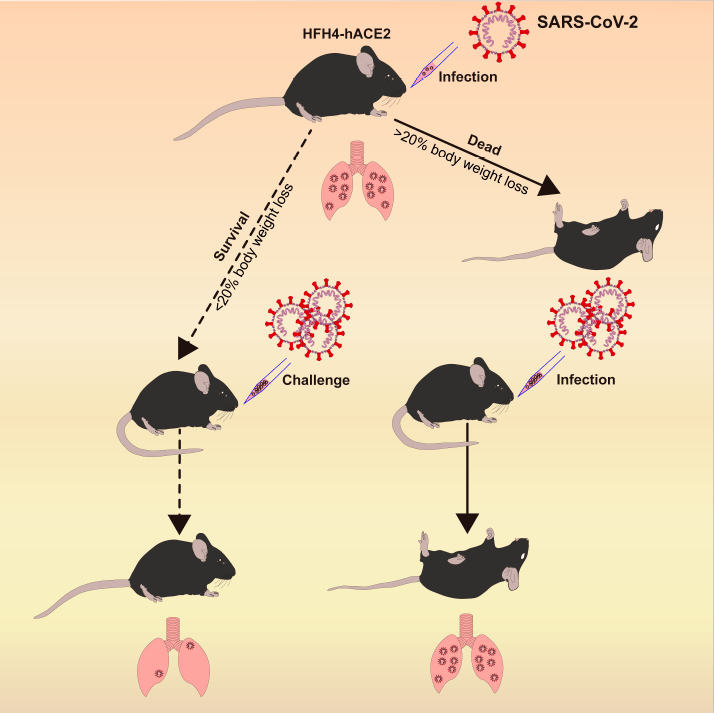
文章模式图(图源自Cell )
由于SARS-CoV-2与严重急性呼吸系统综合症冠状病毒(SARS-CoV)高度同源,通过分子生物学分析发现,SARS-CoV-2与人类血管紧张素转化酶2(hACE2)结合具有更高的亲和力。但是,现在一直缺乏动物模型,这严重阻碍了药物及疫苗的研发。
该研究成功开发了SARS-CoV-2 hACE2转基因小鼠(在C3B6小鼠中为HFH4-hACE2)感染模型。感染的小鼠产生典型的间质性肺炎和病理,与COVID-19患者相似。病毒定量显示肺是感染的主要部位,尽管在某些小鼠的眼睛,心脏和大脑中也可以发现病毒RNA。
从感染的肺和脑组织中分离出全基因组序列中与SARS-CoV-2相同的病毒。最后,该研究表明预先暴露于SARS-CoV-2可以保护小鼠免受严重的肺炎的侵害。总而言之,该结果表明,hACE2小鼠将成为测试潜在疫苗和治疗剂的有价值的工具。


